◎文╱藥師陳浩銘
根據統計,台灣疫苗覆蓋率約達四成,而南韓與香港約為五成,新加坡達到近八成的覆蓋率,顯示台灣疫苗覆蓋率仍需努力提升。台灣政府相關單位積極取得所有有效的疫苗來源,以充足台灣防疫量能;我國自主研發疫苗通過專家投票表決及政府相關審查後,亦成為台灣民眾的選項之一(EUA相關法源可參照藥事法48-2條),雖然社會上對於實際保護效果有諸多討論,但筆者僅就國內各新冠疫苗安全性議題進行摘述。
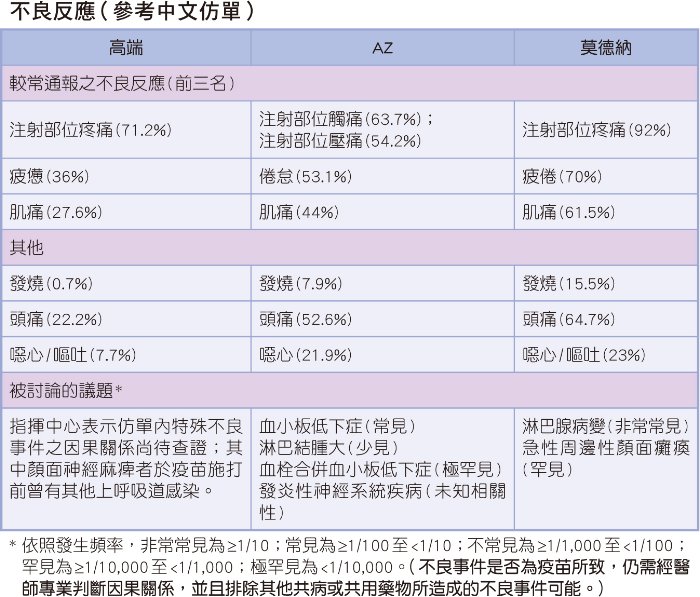
與過往疫苗使用的平台技術不同,AZ疫苗使用黑猩猩腺病毒(chimpanzee adenovirus)作為載體,而莫德納疫苗(Moderna)則以信使核糖核酸(mRNA)作為平台進行病毒棘蛋白轉譯(尚未輸入台灣的輝瑞/BNT疫苗亦使用此種技術);這兩種新的技術在人類疫苗研發使用上屬於較新穎的技術,亦即使用後的長期安全性資料仍屬有限。AZ疫苗的使用,於全球持續有免疫血栓性血小板低下症(VITT)的報導,雖然症狀多屬輕微或中度,並且可以在幾天後得到緩解,但仍有約萬分之一的可能會因此產生血栓而導致嚴重傷害甚至死亡;臨床研究發現其事件發生增加風險之因子包含曾有腦靜脈竇栓塞病史,或是血小板、D-dimer及fibrinogen異常者;歐洲藥品管理局(EMA)亦因此曾發布警示;「AZ疫苗尚未進入美國市場,故US FDA查無相關警訊發布」。莫德納疫苗亦於多國採用,依照各國廣泛使用的經驗,心肌炎(myocarditis)和心包膜炎(pericarditis)是較受關注的不良反應,可能產生的臨床症狀包含呼吸不順、心悸或心律不整、胸痛。我國研發的高端疫苗乃採用次單位蛋白技術平台(recombinant subunit),這是廣泛使用於現有疫苗開發的舊有技術,如B肝疫苗或HPV疫苗等皆用類似技術,該技術的優點是已有長期使用經驗;其較受關注的不良事件包含眼壓升高及顏面神經麻痺,然而相關數據需要更多使用經驗及醫學專家判定,目前資料及生物醫學原理難以確認該不良事件與疫苗是否相關。
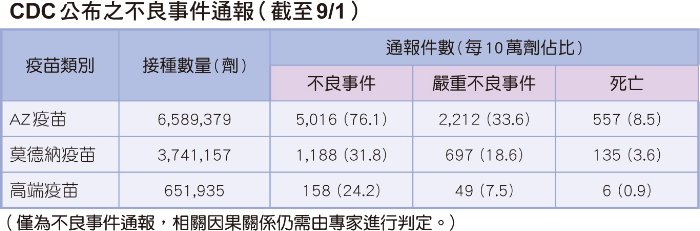
不良反應的評估工具有許多,其主要方式包含時序性、關聯性、專一性(非其他共病或藥物引起)、生物學合理性(可能與藥理或藥物動力學相關)等方式判斷,使用藥品/疫苗後可能的任何事件,應依醫療專業人員從相關資訊進行判定。依據衛福部核准之使用說明書(仿單)記載,注射疫苗常見的不良反應如發燒、頭痛或噁心嘔吐,高端疫苗皆有較低的發生率,而各種疫苗的特殊不良反應則各有不同。此外AZ疫苗中,施打第一劑的不良反應症狀與通報量皆較第二劑高;莫德納疫苗則是第二劑的不良反應通報量較第一劑多;高端疫苗則於仿單中未特別記載。三項疫苗的仿單皆記載年長者的不良反應通報量較少且較輕微。此外,依據疾病管制署發布資訊,截至目前(9/1)新冠肺炎疫苗通報的不良事件約有六千三百多件,嚴重不良事件約有近三千件,疫苗接種後死亡約有近七百件。相關資訊可於疾管署網站查詢。
回首頁 |