
◎文╱藥師張智誠
2021年1月22日,美國FDA批准nivolumab合併cabozantinib的組合,用於晚期腎細胞癌的一線治療,nivolumab是PD-1免疫檢察點抑制劑;cabozantinib是酪胺酸激酶抑制劑(tyrosine kinase inhibitor,TKI),作用於VEGFR、c-MET、AXL等多個靶點。這項批准,成為繼pembrolizumab合併axitinib、avelumab合併axitinib之後,美國FDA核准的第三個免疫檢查點抑制劑合併TKI用於晚期腎細胞癌的治療組合。
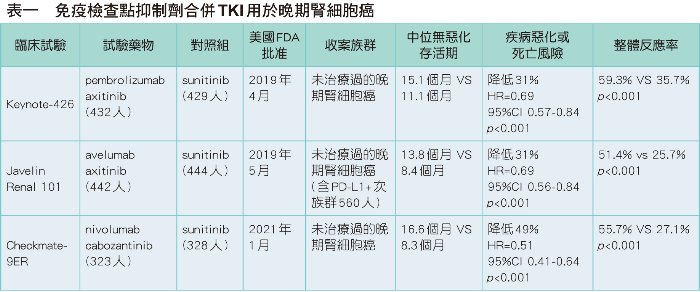
CHECKMATE-9ER是一項隨機、開放標籤試驗,先前未接受過治療的晚期腎細胞癌病人,隨機分派至每兩週接受一次nivolumab 240 mg靜脈輸注30分鐘,合併cabozantinib 40 mg每天口服一次;或每天50 mg sunitinib口服一次。治療四週,然後休息兩週,以六週為一個療程,直到疾病進展或無法接受的毒性為止。Nivolumab合併cabozantinib組,相較於目前晚期腎細胞癌的標準治療sunitinib組,有較佳的中位無惡化存活期、整體存活期,及整體反應率。目前美國FDA核准的免疫檢查點抑制劑合併TKI治療組合用於晚期腎細胞癌,詳列於表一。
接受nivolumab和Cabozantinib聯合治療最常見的不良反應(≥20%)為腹瀉、疲勞、肝毒性、手足症候群、口腔炎、皮疹、高血壓、甲狀腺功能低下、肌肉骨骼疼痛、食慾不振、噁心、消化不良、腹痛、咳嗽和上呼吸道感染等。聯合治療的建議劑量為nivolumab每兩週240mg靜脈輸注30分鐘或每四週480 mg靜脈輸注30分鐘,合併cabozantinib 40 mg每天口服一次,治療四週、休息兩週,以六週為一個療程,直到疾病進展或無法接受的毒性為止。美國FDA公告內容詳見QR Code連結。
參考資料:
1. Brian I Rini, Elizabeth R Plimack, Viktor Stus, et al: Pembrolizumab plus Axitinib versus Sunitinib for Advanced Renal-Cell Carcinoma. N Engl J Med. 2019; 380(12): 1116-27.
2. Robert J Motzer, Konstantin Penkov, John Haanen, et al: Avelumab plus Axitinib versus Sunitinib for Advanced Renal-Cell Carcinoma. N Engl J Med. 2019; 380(12): 1103-15.
回首頁 |