【本刊訊】
「戰備藥品」須依災害防救醫療物資調度支援系統申報數量,進行備藥數量管理,避免在遇到疫情或重大事件時,救命藥會無藥可用。
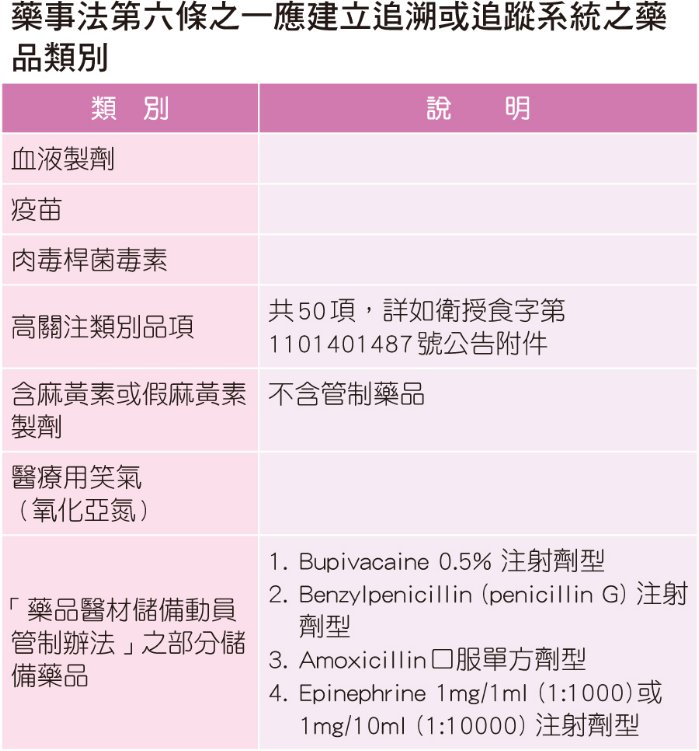
食藥署於5月4日,依據藥事法第六條之一第一項,公告修正「藥事法第六條之一應建立追溯或追蹤系統之藥品類別」,將四款戰備藥品納入藥品追溯或追蹤的應申報品項。這四項藥品,分別是局部麻醉注射劑Bupivacaine 0.5%、抗生素注射劑 Benzylpenicillin (penicillin G)、單方口服抗生素Amoxicillin、過敏休克急救注射劑Epinephrine 1mg/1ml (1:1000)或1mg/10ml (1:10000)。須確保這些藥品在各大醫院備有一定存量,避免流通時出現問題;新制將於今年7月1日起正式實施。
食藥署藥品組簡任技正黃琴喨表示,目前國內已列為應建立追溯或追蹤系統的藥品類別有5大類,第一類為血液製劑、疫苗與肉毒桿菌;第二類為使用量大,受高度關注之藥品;第三類為麻黃素類藥品,其可能遭不當使用,被濫用於製毒;第四類為近年濫用情形嚴重的醫療用笑氣,以及新增的第五類─戰備藥品。
黃琴喨更說明,本次列入追溯與追蹤的四款藥品是依「藥品醫材儲備動員管制辦法」所列的25項戰備藥品中,近2年內曾通報短缺的的品項,因此優先挑選納入追溯追蹤管理。
新制實施後,藥品許可證持有藥商、從事該類製劑批發業務的販賣業藥商,應於每月10日前將上月份藥品追溯或追蹤資訊,上傳至食藥署所建置的藥品追溯或追蹤申報系統。如有未依規定申報者,可依藥事法第92條處3萬元至200萬元的罰鍰。
回首頁 |