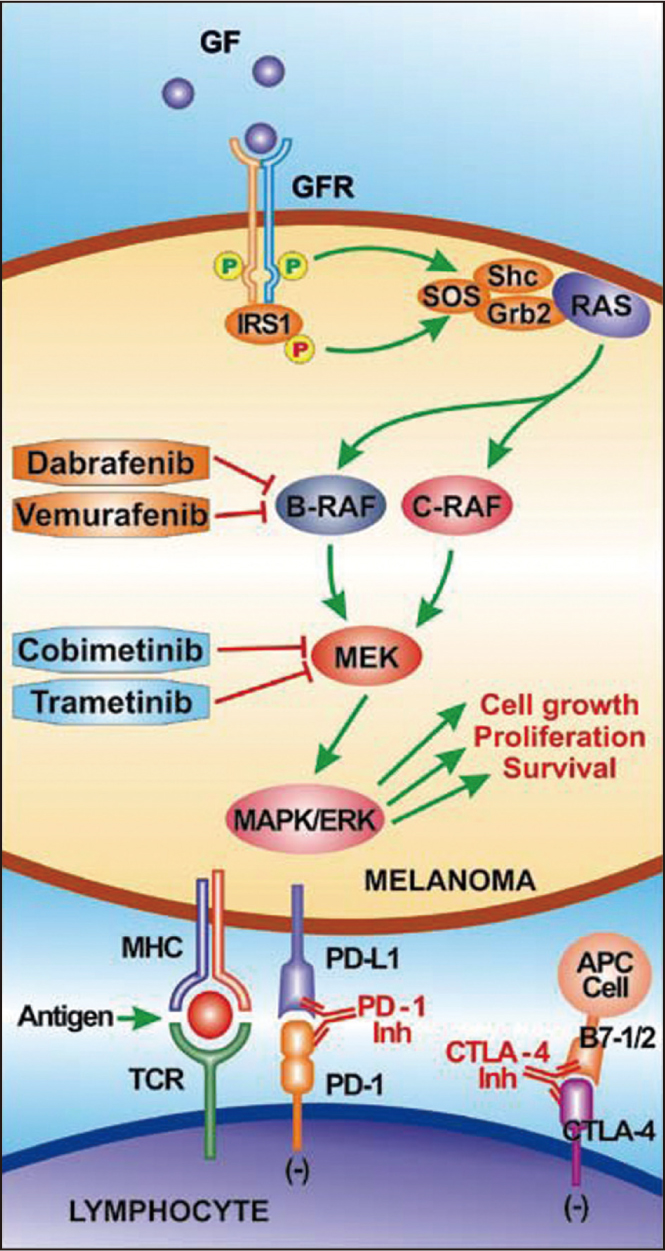
↑圖一 黑色素瘤標靶藥物作用機轉。 (資料來源:參考資料1)

◎文╱台中記者張智誠
黑色素瘤大約一半病例帶有BRAF突變。BRAF和MEK1/2信號通路的異常活化被認為在黑色素瘤及其他類型癌症的發生中發揮了重要作用。Dabrafenib(TafinlarⓇ,泰伏樂)是作用於BRAF的標靶藥物,trametinib(MekinistⓇ,麥欣霓)是作用於MEK的標靶藥物,dabrafenib與trametinib聯合用藥,可以有效地減緩腫瘤生長。黑色素瘤標靶藥物作用機轉如圖一。
第三期黑色素瘤中,腫瘤已經擴散到局部淋巴結,復發或轉移的風險很高,對高危險黑色素瘤病人給予術後輔助治療,可以降低日後復發的風險。第三期臨床試驗COMBI-AD,收入870位BRAF突變、手術切除後的第三期黑色素瘤受試者,以1:1的方式隨機分派至每天口服dabrafenib 150mg BID合併trametinib 2mg QD或安慰劑組,直至疾病復發或無法接受的毒性為止,最長可使用一年,試驗終點為無復發存活期。
Dabrafenib合併trametinib組收入438位受試者,五年無復發存活率為52%;安慰劑組收入432位受試者,五年無復發存活率為36%。Dabrafenib合併trametinib組相較於安慰劑組,可以減少49%疾病復發或死亡的風險(hazard ratio=0.51,95%CI 0.42-0.61,P<0.001)。在安全性方面,dabrafenib與trametinib合併治療最常見的不良反應為發熱、疲勞、噁心、頭痛、發冷、腹瀉、嘔吐、皮疹、關節痛和肌肉疼痛等。
另一第三期臨床試驗COMBI-v,收入704位BRAF突變、不曾治療過的轉移性黑色素瘤受試者,以1:1的方式隨機分派至每天口服dabrafenib 150mg BID合併trametinib 2mg QD或目前的標準治療vemurafenib 960mg BID,直至疾病復發或無法接受的毒性為止,試驗終點為整體存活期。Dabrafenib合併trametinib組收入352位受試者,1年整體存活率為72%;vemurafenib組收入352位受試者,1年整體存活率為65%。Dabrafenib合併trametinib組相較於vemurafenib組,可以減少31%死亡的風險(hazard ratio=0.69,95%CI 0.53-0.89,P=0.005)。
健保將於110年3月1日起開始給付dabrafenib 和trametinib 併用於:(1)治療BRAF V600 突變陽性ECOG? 2且罹患無法切除(第ⅢC期)或轉移性(第Ⅳ期)黑色素瘤之病人,需經事前審查核准後使用,每次申請療程以3個月為限。(2) BRAF V600突變陽性且完全切除之第三期黑色素瘤病人術後輔助治療,需經事前審查核准後使用,每次申請療程以六個月為限,限用一年。健保規範詳見QR code連結。
參考資料
1. Giulia C Leonardi, Luca Falzone, Rossella Salemi, et al: Cutaneous melanoma: From pathogenesis to therapy (Review). Int J Oncol. 2018; 52(4): 1071-80.
2. Reinhard Dummer, Axel Hauschild, Mario Santinami, et al: Five-Year Analysis of Adjuvant Dabrafenib plus Trametinib in Stage III Melanoma. N Engl J Med. 2020; 383(12): 1139-48.
3. Caroline Robert, Boguslawa Karaszewska, Jacob Schachter, et al: Improved overall survival in melanoma with combined dabrafenib and trametinib. N Engl J Med. 2015; 372(1): 30-9.
(本文作者為亞洲大學附屬醫院藥劑科藥師)
回首頁 |