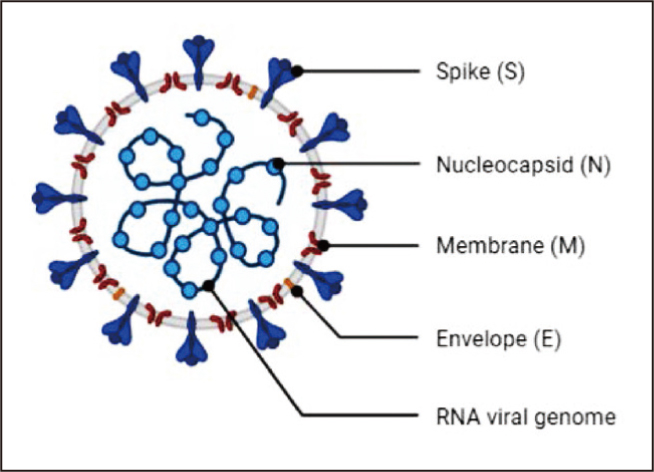
↑圖一 新冠病毒構造。

↑圖二 mRNA 疫苗機轉。
◎文/藥師張基元
新冠肺炎病毒於年初開始肆虐全球,截至11月為止全球感染人數攀升至5565萬人次,死亡人數超過130萬人1,其中以美國(1160萬人感染、25萬人死亡)、印度(896萬人感染、13.2萬人死亡)、巴西(595萬人感染、16.7萬人死亡)災情最為嚴重。
邁入冬季時節,近期歐洲、美洲確診人數也邁入第二個高峰感染期,新冠病毒疫苗研發是現今全球引頸期盼,11月初Pfizer/Biotech公布所研發之疫苗臨床試驗phase 3 初步結果顯示,疫苗(BNT162)能有94~95%抗新冠病毒效力;一周後Moderna也宣布自家疫苗(mRNA-1273)在phases 3 初期結果也能高達94.5%抗新冠病毒效力。整體而言,新冠病毒疫苗研發朝向樂觀可期發展。
新冠病毒疫苗(mRNA疫苗)
目前兩大研發團隊皆選擇mRNA作為疫苗開發,有別於傳統流感疫苗以雞蛋或哺乳類細胞做病毒培養,需要經過繁瑣減毒、純化、病毒培養的過程,動輒耗時半年以上。mRNA 疫苗是分析病原體目標蛋白後,進行基因體定序,接者透過生物資訊大數據及電腦輔助分析設計出雙股plasmid DNA,藉由噬菌體RNA聚合酶體外大量轉錄出mRNA 疫苗,經過純化、GMP(良好作業規範)品管,數天內即可完成疫苗製作2。新冠病毒外裹蛋白質外殼,其殼上有尖刺狀的(spike-like)蛋白,內部遺傳物質為單股RNA,mRNA疫苗基因體資訊來自病毒外殼特殊尖刺狀的(spike-like)蛋白(圖一),因其易於被免疫細胞辨識,模擬其蛋白特性製作設計出無毒性之尖刺蛋白,進而將該目標蛋白生物資學轉換成mRNA(coding sequence, CDS)編碼序列;在5’端加上Cap利於RNA 聚合酶辨認,確保轉譯時方向性;在3’端加上 Poly A,保護序列不易裂解;前後加上兩段非轉譯序列(untranslated region, UTR)調控轉譯過程效率3。
mRNA疫苗機轉
mRNA 疫苗原理是將人體細胞當作疫苗的製造中心(圖二),①mRNA透過微脂體劑型運送至人體細胞周圍,被細胞吞噬入內後,②mRNA 複製酶(replicase)的蛋白表現出來後,促進目標RNA 複製。③大量mRNA透過核醣體轉譯出目標無毒性之尖刺蛋白。④ ⑤部分的目標蛋白也可以成為細胞膜上穿膜蛋白或是分泌至胞外,B cell 辨識後分化成漿細胞、Memory B cell,大量製造抗體,因此日後體內出現目標蛋白外殼的病毒,B cell 被活化產生大量抗體中和抗原,最後病毒被抗體包裹成免疫複合物,被體內吞噬細胞吞噬。⑥目標蛋白可以走向抗原呈現的路徑(antigen-presenting pathway),將蛋白片段性質被MHC-1 受器呈現在胞外,在樹突細胞辨識目標蛋白後能活化T 細胞,使得immature CD4+成熟為 Th1/ Th2 (Helper T cell),也使immature CD8+成熟為自然殺手細胞(cytotoxic T cell),自此體內出現目標蛋白外殼的病毒,T cell 會活化促使病毒死亡。⑦ mRNA 疫苗透過宿主免疫細胞產生特異性抗體。
資料來源
1. WHO統計數據。
2. Giulietta Maruggi , Cuiling Zhang , Junwei Li , Jeffrey B Ulmer, Dong Y. mRNA as a Transformative Technology for Vaccine Development to Control Infectious Diseases Mol Ther. 2019 Apr 10;27(4):757-772.
3. Nicholas A C Jackson , Kent E Kester , Danilo Casimiro , Sanjay Gurunathan , Frank DeRosa The promise of mRNA vaccines: a biotech and industrial perspective. NPJ Vaccines. 2020 Feb 4;5:11.
回首頁 |