
◎文╱台中記者張智誠
急性骨髓性白血病(AML)俗稱血癌,治療上以化學治療及造血幹細胞移植為主,雖然大部分的病人接受化療後可以獲得緩解,但多數病人會再復發,僅少數病人可以治癒,如何改善病人的治療成效,仍是目前重要的課題。AML與多種基因突變有關,FLT3突變是其中之一,FLT3突變會導致AML病人的預後不良。
Midostaurin(RydaptⓇ,療德妥)是一個多重靶點的酪胺酸酶抑制劑,同時作用於KIT與FLT3等多個靶點,於2017年4月獲得美國FDA核准,用於治療FLT3突變陽性的新診斷AML成年病人,midostaurin成為全球第一個一線治療FLT3突變陽性AML的標靶藥物。台灣FDA也於2018年4月核准midostaurin,核准的適應症為:新確診為FLT3突變陽性的AML成年病人之標準前導(daunorubicin併用cytarabine)與鞏固性化療(高劑量cytarabine)時合併使用。
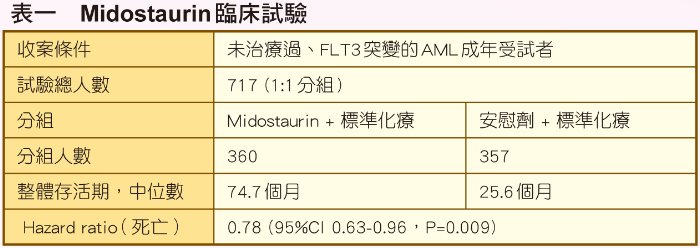
一項第三期臨床試驗,從未治療過的3277位成年(18-59歲)AML病人中篩選出717位FLT3突變的受試者,以1:1的比例隨機接受口服midostaurin 50 mg Q12H(每個療程的第8-21天)合併標準化療(前導化療:daunorubicin合併cytarabine,1-2個療程;鞏固性化療:高劑量cytarabine,共4個療程)或安慰劑合併標準化療,疾病緩解之後的維持治療繼續每天併用midostaurin 50 mg Q12H或安慰劑,維持治療以28天為一個療程,共12個療程,試驗終點為受試者的整體存活期(overall survival,OS)。
Midostaurin加標準化療組整體存活期的中位數為74.7個月,安慰劑加標準化療組整體存活期的中位數則為25.6個月,Midostaurin加標準化療組相較於安慰劑加標準化療組可以降低22%死亡的風險(HR=0.78,95%CI 0.63-0.96,P=0.009)。標準化療加上midostaurin治療,可以延長受試者的整體存活期。
兩組常見的副作用皆為:貧血、嗜中性白血球低下、血小板低下、淋巴球減少、嗜中性白血球低下合併發燒、感染、腹瀉、低血鉀等,midostaurin加標準化療組有較多貧血及皮疹的副作用(P<0.05)。
健保於109年2月1日開始給付midostaurin,為AML的治療帶來新契機,midostaurin限用於新確診為FLT3突變陽性的AML成年病人之標準前導與鞏固性化療時合併使用,且需排除急性前骨髓性細胞白血病(APL)的病人,每人以總共給付6 個療程為上限,若病人接受造血幹細胞移植後則將不再給付本藥品。(給付條件與公告內容詳見QR Code連結)
參考資料:
Stone RM, Mandrekar SJ, Sanford BL et al: Midostaurin plus Chemotherapy for Acute Myeloid Leukemia with a FLT3 Mutation. N Engl J Med. 2017; 377(5): 454-64.
回首頁 |