|
◎文╱臺中記者李亞芝
衛福部食藥署於2025年年初發布「全身作用性維生素B12類藥品之風險再評估結果相關事宜」,公告凡持有相關藥品許可證之藥商應限期完成中文仿單變更。
維生素B12類藥品及其製劑(例如cyanocobalamin、
hydroxocobalamin、cobamamide、mecobalamin)常用於治療惡性貧血、巨胚紅血球性貧血、末梢神經障礙、神經炎、維生素B12
缺乏症等疾病。英國醫藥品管理局(Medicines and Healthcare products Regulatory Agency,
MHRA)於2023年底發布安全資訊,表示由於維生素B12(vitamin
B12)的結構中含有鈷(cobalt),建議已知對鈷過敏的病人使用含維生素B12類藥品時應抱持警覺。
食藥署表示,一般群體中估計約1-3%的人可能對鈷過敏。鈷敏感反應通常以慢性或亞急性過敏性接觸性皮膚炎等皮膚症狀呈現,但鈷過敏也可能罕見地誘發類似多型性紅斑的反應;症狀可能在用藥後立即發生或延遲於給藥後的72小時內發生。
衛生福利部核准之藥品許可證單/複方共304張,中文仿單未提及對鈷過敏之病人應留意過敏反應等相關安全資訊,因此公告包含處方藥及非處方藥全身作用性維生素B12類藥品之中文仿單應加註警語,以提昇醫療人員及民眾對於相關藥品之警覺性。
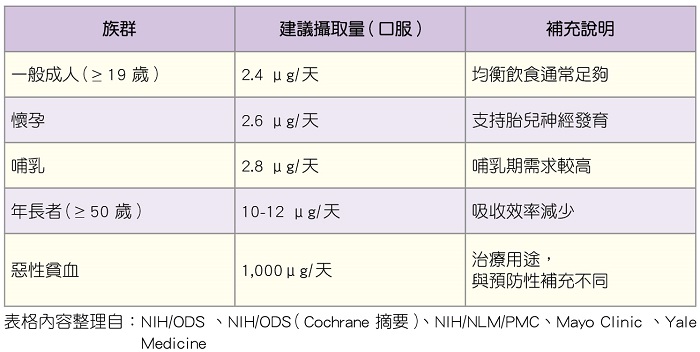
針對不同族群的維生素B12每日攝取劑量如下表:
資料來源:
1.公告全身作用性維生素B12類藥品之風險再評估結果相關事宜。 - 本署公告 - 公告資訊 - 衛生福利部食品藥物管理署
2.全身作用性維生素B12(vitamin B12)類藥品安全資訊風險溝通表 – 藥害救濟基金會
回首頁 |