
◎文╱台中記者張智誠
Brigatinib(AlunbrigR,癌能畢)是第三代的ALK抑制劑,2017年4月美國FDA核准brigatinib。核准的適應症為:在crizotinib治療中惡化或無法耐受之ALK陽性的晚期非小細胞肺癌病人,台灣FDA也於108年8月核准brigatinib,核准的適應症與美國FDA相同。
第三期臨床試驗,收入未使用過ALK抑制劑的ALK陽性晚期非小細胞肺癌受試者,比較口服brigatinib 180mg QD(前7天90mg QD)與crizotinib 250mg BID的療效與安全性。此試驗共收入275位受試者,以1:1的方式隨機分配至brigatinib組或crizotinib組,試驗終點為無惡化存活期(progression-free survival, PFS)。
Brigatinib組共收入137位受試者、crizotinib組共收入138位受試者。Brigatinib組的十二個月無惡化存活率為67%(95%CI 56-75),crizotinib組的十二個月無惡化存活率為43%(95%CI 32-53),brigatinib組相較於crizotinib組,可以減少51%疾病惡化或死亡的風險(hazard ratio 0.49,95%CI 0.33-0.74,P<0.001)。在安全性方面,兩組都沒有發現新的安全性訊號。
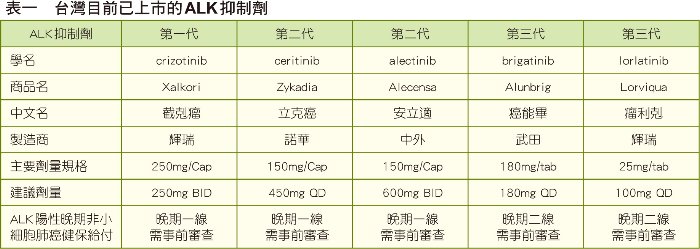
健保於109年8月1日開始有條件給付brigatinib,90mg健保價2,803元,180mg健保價5,046元。Brigatinib適用於在crizotinib 治療中惡化之ALK 陽性的晚期非小細胞肺癌病人,須經事前審查核准後使用。每次申請事前審查之療程以三個月為限,每三個月需再次申請,再次申請時並需附上治療後相關臨床資料,若病情惡化即不得再次申請。健保給付條件與公告內容詳見QR Code連結。台灣目前已上市的ALK抑制劑如表一。
參考文獻:
D Ross Camidge, Hye Ryun Kim, Myung-Ju Ahn, et al: Brigatinib versus Crizotinib in ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med 2018; 379(21): 2027-39.
回首頁 |